Capítulo 21
Control de Calidad
Las pruebas de control de calidad (QC) son una parte importante del trabajo de rutina de medicina nuclear. Se deben realizar a intervalos de tiempo designados para mantener la funcionalidad adecuada de la cámara gamma. QC es una parte constitutiva del programa de gestión de calidad del departamento de medicina nuclear. A continuación se muestra una lista de las pruebas involucradas en el control de calidad para la cámara gamma y la TC. Las pautas sobre los procedimientos de control de calidad deben estar disponibles para todos los tecnólogos que realizan estas pruebas.
Pruebas de constancia: aquellas pruebas realizadas para determinar variaciones en los datos de referencia, que describen el equipo, sus componentes individuales y el estado inicial. Estos son realizados por el operador del equipo.
Pruebas de aceptación: afirman que los parámetros de rendimiento del equipo satisfacen las especificaciones técnicas, legales y/o del fabricante. Estos son realizados por el fabricante del equipo.
Niveles de acción: valores utilizados en pruebas de constancia. Si se superan esos valores, se debe realizar una investigación de acuerdo con el marco de gestión de la calidad.
Límites de tolerancia: si se exceden, el uso del equipo en la rutina clínica está limitado o posiblemente no permitido. Las violaciones de los límites de tolerancia, sus causas y consecuencias deben ser documentadas y justificadas por el oficial de protección radiológica.
Mantenimiento de registros: se debe registrar la documentación de los procedimientos y resultados del control de calidad, junto con la fecha y las iniciales de la persona que realiza la prueba.

D – Diario, W/M – Semanal/mensual, M – Mensual, Q – Trimestral
Pruebas diarias
La inspección visual y física de la cámara gamma SPECT debe detectar defectos o daños mecánicos o eléctricos externos. Se debe realizar una prueba de almohadilla táctil diariamente y después de cada cambio de colimador. Se debe realizar una verificación operativa adicional en los botones de parada de emergencia, si está disponible, que deben encender y apagar todos los movimientos del sistema accionado por motor cuando se presiona.
Como se muestra en la Figura 1, el ajuste de ventana para el radionúclido a usar debe realizarse, por ejemplo 99m Tc, para asegurar que el pico para el radiofármaco seleccionado coincida con el objeto debajo de la cámara. Si esto no se realiza, puede producirse la degradación de la calidad de la imagen y la pérdida de resolución espacial.

La verificación operativa de las tasas de recuento de antecedentes con o sin colimadores y dentro de una o más ventanas de energía debe realizarse diariamente para detectar la radiación causada por la posible contaminación radiactiva de la cámara de centelleo o el entorno, la radiación externa de una fuente no protegida vecina o un exceso de ruido electrónico.
La uniformidad extrínseca del equipo de imagen debe realizarse diariamente para acceder a la respuesta del sistema al flujo espacialmente uniforme de los fotones 57 153 Gd. Dicha uniformidad del campo de inundación puede probarse cualitativamente mediante inspección visual o cuantitativamente mediante el cálculo de la uniformidad de la imagen integral y diferencial dentro del campo de visión central (CFOV) de la cámara y el campo de visión útil (UFOV). La Figura 2 demuestra un ejemplo de uniformidad extrínseca usando 57 Co, que es una fuente de inundación externa.

Pruebas semanales/mensuales
Uniformidad intrínseca
La uniformidad intrínseca implica realizar la prueba de control de calidad sin ninguna variable, como colimadores, para comprobar la respuesta de los sistemas al flujo espacialmente uniforme de 99m Tc. La Figura 3 muestra un ejemplo del resultado final conseguido después de realizar una prueba de uniformidad intrínseca.

Figura 3. Un ejemplo de un informe de una prueba de uniformidad intrínseca
Centro de Rotación
El centro de rotación (COR) es el punto en el que se interceptan el eje de rotación de la cámara gamma y el centro perpendicular del plano detector. La alineación transaxial de las imágenes de proyección adquiridas con el centro mecánico de rotación del sistema es crítica para la generación precisa de imágenes tomográficas reconstruidas a partir de imágenes de proyección adquiridas. Para el sistema SPECT de múltiples cabezas, es crucial que el centro electrónico de cada proyección angular utilizado en el proceso de reconstrucción de imágenes esté alineado consistentemente con el centro de rotación mecánica. Como se muestra en la figura 4, las fuentes puntuales se colocan en un fantasma, por lo que la cámara gamma gira alrededor de este fantasma, produciendo un resultado como se muestra en la figura 5 (este ejemplo ilustra un procedimiento específico requerido por el fabricante, pueden existir otras configuraciones).

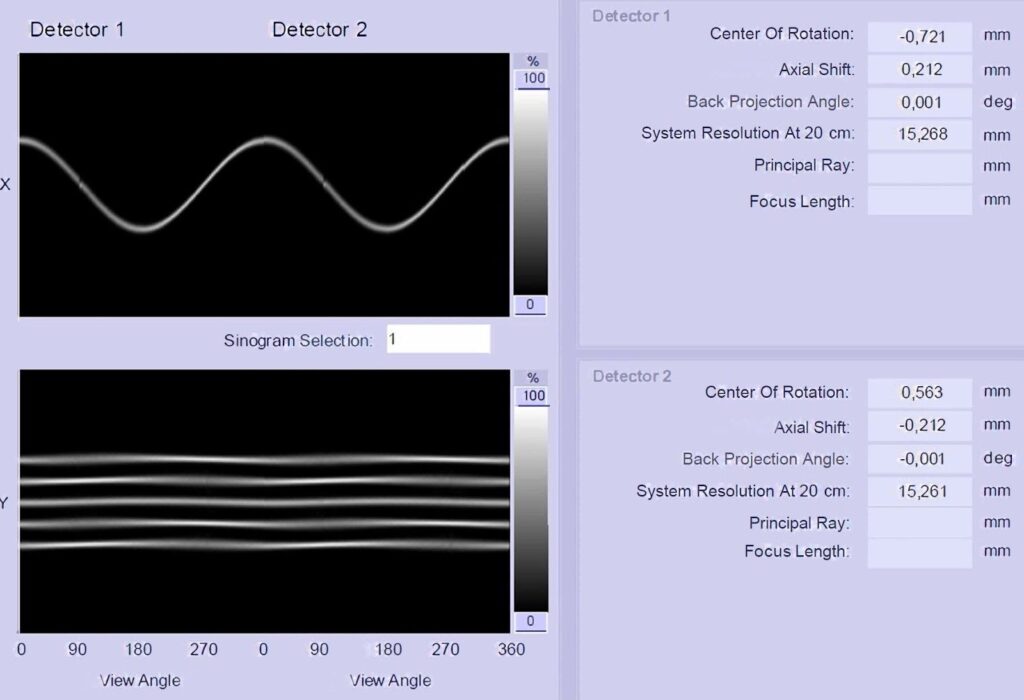
Resolución espacial y linealidad
La resolución espacial es la capacidad de una cámara de centelleo para resolver con precisión fuentes radiactivas separadas espacialmente. El propósito de verificar la resolución espacial y la linealidad es detectar el deterioro gradual a largo plazo de la resolución espacial, y mostrar los objetos lineales de la imagen lo más exactamente lineales posible, en comparación con las mediciones de aceptación y referencia, mostradas en la Figura 6. La adquisición de imágenes fantasma de la barra puede o no ser requerida por los fabricantes de equipos de imagen, pero se realiza a discreción del usuario. Un ejemplo del fantasma de la barra utilizado para la resolución espacial y la linealidad se muestra en la figura 7.


La realización de exámenes SPECT/CT presenta desafíos como el desajuste, que degradan la precisión con la que el SPECT está alineado con la TC. Un ejemplo de una fabricación se describirá aquí:
El control de calidad de SPECT/CT generalmente implica varias fuentes (es decir, fuentes puntuales, un fantasma con esferas o fuentes de línea oblicua) que contienen el material de contraste utilizado para CT y una fuente puntual del radionúclido 99m Tc, colocado en fuentes puntuales de plástico, como se muestra en la figura 8. Se realiza una adquisición de SPECT/CT, seguida de las reconstrucciones habituales implicadas, como se muestra en la Figura 9. La desviación permitida entre SPECT y CT no debe exceder los 5mm. Se respetan las especificaciones del fabricante.
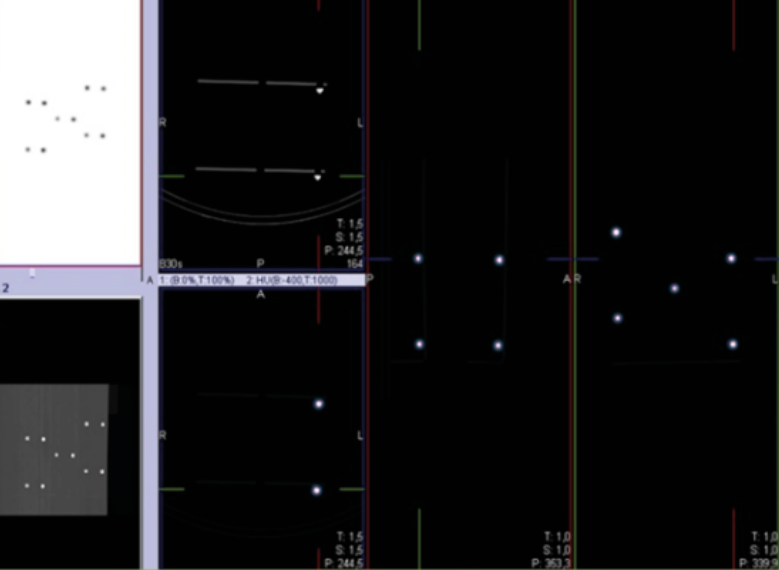

SPECT Calidad de imagen
Un fantasma de rendimiento total de SPECT está diseñado para proporcionar una evaluación cualitativa de las imágenes tomográficas y un procedimiento de control de calidad para demostrar el límite de rendimiento del sistema SPECT. El fantasma SPECT más utilizado, el fantasma ‘Jaszczak’, contiene un contenedor cilíndrico para simular el abdomen del paciente. Dentro del fantasma, hay una serie de esferas sólidas y varillas de diámetros variables. El contenedor uniforme del fantasma se utiliza generalmente para detectar artefactos de anillo (que surgen de la falta de uniformidad del detector), mientras que las esferas y varillas se utilizan para evaluar el contraste y la resolución de estimación. En un ajuste de cámara gamma, el fantasma se llena típicamente con alrededor de 300 MBq de 99m Tc (de acuerdo con el colimador que se va a usar) para crear un fondo de actividad uniforme, el fantasma se escanea a continuación durante aproximadamente 15-30 minutos para obtener una adquisición de SPECT de alto recuento. Las esferas también podrían llenarse con cantidades fijas de actividad para realizar una prueba “caliente”. Por ambos métodos, la resolución de contraste y la resolución espacial del sistema se pueden determinar a partir de los resultados. Un ejemplo del fantasma ‘Jaszczak’ se muestra en la Figura 10. Otros fantasmas como el fantasma de Carlson también se pueden utilizar para lograr los mismos resultados que los anteriores.



Alineación de PET/CT (1/2 año)
Otra opción para hacer esta prueba es el uso de la actividad intrínseca de los cristales LSO en los sistemas de detectores de PET digitales. Aquí, el sistema detector muy sensible cuenta los eventos por esa actividad intrínseca muy baja de la fracción de 176Lu en el material de LSO. Actualmente, no todos los fabricantes de PET-Systems digitales ofrecen esa opción. La Figura 12 ilustra un ejemplo de este fantasma, y la Figura 13 ilustra el resultado de la exploración, listo para la evaluación visual.


La EANM fomenta la implementación de un programa para que los centros empleen la garantía de calidad y el control de calidad requeridos para obtener la acreditación EARL (EANM Research Limited) earl.eanm.org. Su objetivo es armonizar el control de calidad realizado en diferentes centros que están dispuestos a ser acreditados por EARL, estandarizando así el control de calidad realizado y logrando resultados que puedan cuantificarse. Los centros acreditados por EARL pueden intercambiar hallazgos y datos, incluida la preparación del paciente.
Tomografía Computarizada (TC)
La tomografía computarizada utilizada con fines de diagnóstico debe someterse a pruebas de control de calidad para funcionar dentro de límites aceptables.

La prueba diaria de control de calidad de TC de rayos X del sistema de TC debe realizarse de acuerdo con los procedimientos recomendados por el fabricante y el asesoramiento experto de los físicos médicos. Está implícito que las siguientes pruebas se aplican a las aplicaciones de TC de diagnóstico estándar, la demanda de control de calidad puede relajarse en el caso de la TC solo de corrección de atenuación (AC) o extender, por ejemplo, en aplicaciones de radioterapia.
Por ejemplo, se puede recomendar realizar procedimientos diarios de calidad de CT que ejecuten automáticamente un conjunto de adquisiciones de calentamiento de tubo de CT, comprobaciones automáticas de función y diferentes pasos de calibración de aire y agua para todos los ajustes de voltaje disponibles, con el fin de garantizar una calidad de imagen óptima. La alineación con láser debe verificarse al principio del día. La alineación con láser debe coincidir con las ranuras en el fantasma antes de realizar el control de calidad.
De acuerdo con las instrucciones del fabricante, el calentamiento del tubo se debe realizar después de un corto tiempo en que el tubo CT ha estado inactivo, y también se debe realizar una calibración del tubo de TC todos los días, ya sea al principio o al final del día, y documentarse. Un ejemplo de una imagen de CT homogénea de un fantasma de agua se muestra en la Figura 14 (A). En la Figura 14 (B), se demuestra un artefacto de anillo, que es antiestético cuando se realizan exámenes.


Procedimientos de control de calidad sin imágenes realizados en medicina nuclear
Medidor De Actividad, Contadores De Pozo
La regulación de la protección contra la radiación en medicina requiere la implementación de procedimientos regulares de garantía de calidad también para los calibradores de dosis. La verificación regular de la precisión, confiabilidad y constancia de las mediciones de actividad en las instalaciones de medicina nuclear es esencial para la seguridad del paciente, ya que las lecturas de actividad incorrectas pueden resultar directamente en una sobredosis o una dosis insuficiente y, por lo tanto, comprometer el resultado clínico de los procedimientos diagnósticos o terapéuticos. Como parte de las pruebas, las mediciones de actividad se realizan usando una fuente de referencia adecuada, y los valores medidos se comparan con los valores de referencia específicos de nucleido, que normalmente son establecidos por el fabricante o proveedor del calibrador de dosis durante la prueba de aceptación o una inspección de seguridad posterior.
Además, se debe observar la verificación del avance del molibdeno-99 para los metros de actividad utilizados para la medición del tecnecio-99m, lo que requiere la presencia de un blindaje adicional específico.
Las pruebas de constancia diarias de los medidores de actividad deben incluir la verificación tanto del fondo como de la respuesta en un entorno de nucleido/energía particular.
La verificación de antecedentes sirve para excluir tasas excesivas de recuento de antecedentes, contaminación de la cámara de ionización o soporte de muestra, y para verificar la función electrónica adecuada de la cámara de ionización. Para este propósito, se debe realizar una medición de actividad en el entorno de nucleidos más utilizado sin ninguna fuente radiactiva en la cámara.
La verificación de la constancia de la respuesta, y por lo tanto la calibración de la señal al valor de actividad absoluta, debe realizarse diariamente utilizando el mismo ajuste de nucleido que el utilizado durante la prueba de aceptación. La actividad de una fuente de referencia de larga duración se determina y se compara con el valor de referencia correspondiente establecido durante la prueba de aceptación del calibrador de dosis. La desviación relativa del valor medido no debe exceder el nivel de acción (generalmente el 3%) o el límite de tolerancia (generalmente el 5%).
La fuente de referencia utilizada debe estar sellada, tener una actividad conocida, una semivida superior a cinco años y una alta pureza radionuclídica. En la práctica, se usa comúnmente una fuente de referencia de cesio-137 (vida media: 30,2 años).
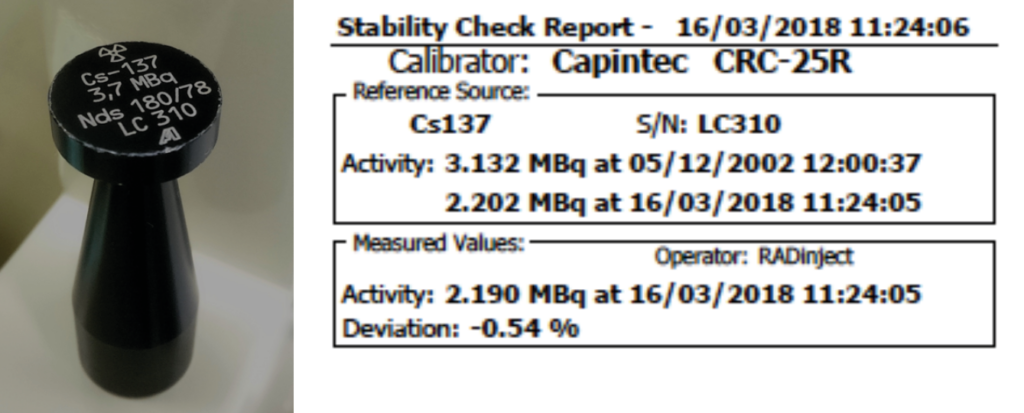
Si se utiliza un generador más de aproximadamente 14 días después de la elución inicial, se recomienda una prueba repetida del avance del molibdeno.
El eluato se mide una vez que utiliza el ajuste technetium-99m, y una vez que se utiliza el dispositivo de blindaje especial suministrado para la prueba de avance.
La fracción de molibdeno en el eluato no debe exceder el 0,1 %.
La mayoría de los fabricantes de medidores de actividad también ofrecen contadores de tipo pozo (o contadores de pozos). Estos son, en esencia, calibradores de dosis especializados diseñados para actividades muy bajas. Se usan para medir la concentración de actividad en muestras tales como muestras de sangre, orina o muestras de pacientes similares con niveles de actividad muy bajos, que típicamente varían de unos pocos kBq a unos 10 y 100 Bq.
Los procedimientos diarios de control de calidad para contadores de pozos corresponden en gran medida a los de los medidores de actividad estándar.
Las pruebas semestrales o menos frecuentes son la comprobación de la linealidad del sistema y deben verificarse al menos cada seis meses utilizando el ajuste de nucleidos más utilizado en un medidor de actividad en particular.
Esta prueba comprueba la linealidad de la medición de la actividad en un amplio rango de actividad midiendo repetidamente una fuente radiactiva de corta duración (p. ej. Technetium-99m o Flúor-18) a intervalos de tiempo definidos y comparando los valores medidos con las actividades esperadas corregidas por desintegración en cada punto en el tiempo.
La desviación relativa entre la actividad medida y la esperada debe estar dentro de la tolerancia (generalmente ± 5%) siendo generalmente el 3% el nivel de acción.
Las pruebas de linealidad deben cubrir un rango de actividad de 1 MBq hasta la actividad máxima del paciente medida con el dispositivo bajo prueba, pero al menos hasta 1 GBq. Los intervalos de medición deben elegirse de manera que se obtengan varias lecturas por década de actividad. Los medidores de actividad modernos están equipados con protocolos de medición que realizan automáticamente la adquisición, análisis y documentación de datos.
Para los contadores de tipo de pozo, el factor de calibración debe determinarse adicionalmente cada seis meses. Esto se define como la relación de la actividad medida en el medidor de actividad a la tasa de recuento medida en el contador de pozo.
Su determinación es necesaria como parte de los controles de calidad semestrales, aunque no se prescribe ningún procedimiento de medición específico. Se pueden aplicar diversos métodos para su determinación.
Sondas para la cirugía guiada por radiactividad (RGS) y la vigilancia de la tasa de dosis
Durante muchos años, los dispositivos de tipo sonda se han utilizado para la detección/localización de áreas y estructuras con captación de radiactividad, por ejemplo, en el contexto de la biopsia de ganglio linfático centinela (SLNB).
Estos instrumentos deben someterse a mediciones diarias de la constancia de fondo y respuesta.
Para este propósito, normalmente se usan fuentes de referencia de cobalto-57 con una actividad nominal de aproximadamente 200 kBq. Los sistemas de sonda disponibles comercialmente se suministran con accesorios dedicados y protocolos de prueba que permiten un rendimiento reproducible de estas comprobaciones.
A intervalos más largos, generalmente cada seis años, el fabricante debe realizar una inspección de seguridad, durante la cual generalmente se establecen nuevos valores de referencia para los controles de constancia diarios.
Si se utilizan sondas gamma fijas (estacionarias), por ejemplo, para medir la biocinética y la acumulación de radionúclidos en el contexto de los procedimientos terapéuticos, estos dispositivos deben verificarse principalmente de acuerdo con las especificaciones del fabricante e inspeccionarse por el fabricante al menos una vez al año.
Cuando tales sondas se utilizan para la monitorización de parámetros cuantitativos, por ejemplo:
Para verificar que las tasas de dosis ambiente en las proximidades de los pacientes (por ejemplo, a una distancia de 2 m) caen por debajo de un criterio de liberación definido de las salas de terapia con radionúclidos, o para cuantificar las acumulaciones de actividad como parte de la verificación físico-técnica de la terapia con radionucleidos, deben calibrarse anualmente usando el radionúclido más comúnmente empleado en terapia.
Instrumentación de RP
Una sonda intraoperatoria se utiliza generalmente para detectar la radiación gamma durante los procedimientos de no formación de imágenes. La inspección física de los cables que se conectan a la sonda real y la evaluación de la tensión del circuito interno se debe realizar antes de cada uso. La sensibilidad y la constancia de la sonda deben ensayarse a intervalos fijos con una fuente radiactiva de referencia. Las recomendaciones del fabricante deben mantenerse a mano, y cada resultado del control de calidad documentado.
Recomendaciones de envoltura
La importancia del control de calidad en los procedimientos de medicina nuclear es esencial para una buena calidad de imagen, así como para la seguridad de la radiación del paciente. Al realizar el control de calidad de rutina, se garantiza un rendimiento de alta calidad del equipo utilizado. La documentación de las pruebas realizadas debe mantenerse y es especialmente importante en el reconocimiento de las tendencias. Los resultados de las pruebas que se encuentran en la sección de «nivel de aceptación» pero que se están moviendo hacia la «sección de nivel de acción» podrían tratarse lo antes posible y antes de que surjan problemas.
Para más información sobre el control de calidad en medicina nuclear, el lector se refiere a las siguientes publicaciones:
BusemannSokole E., Plachćinska A., Britten A., Georgesopoulou M. L., Tindale W., Klett R., “Routine quality control recommendations for nuclear medicine instrumentation”, European Journal of Medical Molecular Imaging, 2010; 37:662-71, [Disponible en línea], http://www.eanm.org/content-anm/uploads/2017/11/EANM_2017TEchGuide_QualityControl.pdf
Asociación Europea de Medicina Nuclear (EANM), (2017) “Control de calidad de la instrumentación de la medicina nuclear y la normalización del protocolo”, [Disponible en línea], http://eanm.org/publications/guidelines/4_EJNMMI_Physics_GL_RoutineQC_fulltext_03_2010.pdf
Comisión Alemana de Protección Radiológica, (2011-2018), “Control de calidad de los equipos de medicina nuclear – Definición de los niveles de acción y los límites de tolerancia”, [Disponible en línea] https://www.ssk.de/SharedDocs/Beratungsergebnisse/2010/Qualitaetskontrolle_nuklearmedizinischeGeraeten.html? nn=2241584
2. Cal-Gonzalez J, Rausch I, Shiyam Sundar LK, Lassen ML, Muzik O, Moser E, et al. Imágenes híbridas: Instrumentación y procesamiento de datos. Front Phys 2018;6. https://doi.org/10.3389/fphy.2018.00047.
3. Wissing MD, van Leeuwen FWB, van der Pluijm G, Gelderblom H. Cloruro de radio-223: prolongación de la vida en pacientes con cáncer de próstata mediante el tratamiento de metástasis óseas. Clin Cancer Res 2013;19:5822–7. https://doi.org/10.1158/1078-0432. CCR-13-1896.
4. Wang F, Casalino LP, Khullar D. Aprendizaje profundo en la medicina-promesa, progreso y desafíos. JAMA Intern Med 2019; 179:293–4. https://doi.org/10.1001/jamainternmed.2018.7117.
5. Kotsiantis SB. Aprendizaje automático supervisado: una revisión de las técnicas de clasificación n.d.:20.
6. Olson RS, Cava WL, Mustahsan Z, Varik A, Moore JH. Asesoramiento basado en datos para la aplicación del aprendizaje automático a problemas de bioinformática. Biocomputación 2018, CIENTÍFICO MUNDIAL; 2017, p. 192–203. https://doi.org/10.1142/9789813233533_0018.
7. Tarca AL, Carey VJ, Chen X, Romero R, Drăghici S. El aprendizaje automático y sus aplicaciones a la biología. PLOS Computational Biology 2007;3:e116. https://doi.org/10.1371/journal.pcbi.0030116..
8. Maaten L van der, Hinton G. Visualización de datos usando t-SNE. Revista de Investigación de Aprendizaje Automático 2008;9:2579–605.
9. Gao Y, Liu Y, Wang Y, Shi Z, Yu J. Un método de estandarización de intensidad universal basado en una red de adversarios de ciclo de emparejamiento débil de muchos a uno para imágenes de resonancia magnética. IEEE Transactions on Medical Imaging 2019;38:2059–69. https://doi.org/10.1109/TMI.2019.2894692.
10. Frid-Adar M, Klang E, Amitai M, Goldberger J, Greenspan H. Aumento de datos sintéticos utilizando GAN para mejorar la clasificación de la lesión hepática. 2018 IEEE 15o Simposio Internacional de Imágenes Biomédicas (ISBI 2018), 2018, p. 289–93. https://doi.org/10.1109/ISBI.2018.8363576
.
11. Chen M, Shi X, Zhang Y, Wu D, Guizani M. Deep Features Learning para el análisis de imágenes médicas con la red neuronal convolucional Autoencoder. IEEE Transactions on Big Data 2017:1–1. https://doi.org/10.1109/TBDATA.2017.2717439.
12. Visvikis D, Cheze Le Rest C, Jaouen V, Hatt M. Inteligencia artificial, aprendizaje automático (profundo) y radio(geno)mics: definiciones y aplicaciones de imágenes de medicina nuclear. Eur J Nucl Med Mol Imaging 2019;46:2630–7. https://doi.org/10.1007/s00259-019-04373-w.
13. Cook GJR, Goh V. ¿Qué puede enseñar la inteligencia artificial sobre los mecanismos moleculares subyacentes a la enfermedad? Eur J Nucl Med Mol Imaging 2019;46:2715–21. https://doi.org/10.1007/s00259-019-04370-z.
14. Hatt M, Tixier F, Visvikis D, Rest CCL. Radiómica en PET/CT: ¿Más de lo que parece? J Nucl Med 2017;58:365–6. https://doi.org/10.2967/jnumed.116.184655.
15. Lambin P, Leijenaar RTH, Deist TM, Peerlings J, de Jong EEC, van Timmeren J, et al. Radiómica: el puente entre la imagen médica y la medicina personalizada. Nature Reviews Clinical Oncology 2017;14:749–762. https://doi.org/10.1038/nrclinonc.2017.141.
16. Valentin, J. Publicación 103 de la CIPR Las recomendaciones de 2007 de la Comisión Internacional de Protección Radiológica. CIP 103 2007; 37.
17. Kratz J, Strasser C. Consenso y controversias de publicación de datos. F1000Res 2014;3:94. https://doi.org/10.12688/f1000research.3979.3.
18. Kalendralis P, Shi Z, Traverso A, Choudhury A, Sloep M, Zhovannik I, et al. Colecciones de RIDER, interobserver, Lung1 y TCIA de TCIA que cumplen con la normativa FAIR y DICOM. Med Phys 2020. https://doi.org/10.1002/mp.14322.
19. Panch T, Mattie H, Celi LA. La “verdad incómoda” sobre la IA en la atención médica. Npj Digital Medicine 2019;2:1–3. https://doi.org/10.1038/s41746-019-0155-4.
20. Zhang L, Yang H, Jiang Z. Clasificación de datos biomédicos desequilibrada utilizando ELM multicapa autoadaptativa combinada con GAN dinámico. BioMedical Engineering OnLine 2018; 17:181. https://doi.org/10.1186/s12938-018-0604-3.
21. Yu H, Hong S, Yang X, Ni J, Dan Y, Qin B. Reconocimiento de múltiples tipos de cáncer desequilibrados basados en datos de micromatrices de ADN utilizando clasificadores de conjunto. BioMed Research International 2013;2013:e239628. https://doi.org/10.1155/2013/239628..
22. Acortar C, Khoshgoftaar TM. Una encuesta sobre el aumento de datos de imágenes para el aprendizaje profundo. Journal of Big Data 2019;6:60. https://doi.org/10.1186/s40537-019-0197-0.
23. Wibmer AG, Hricak H, Ulaner GA, Weber W. Tendencias en la imagen híbrida oncológica. European Journal of Hybrid Imaging 2018;2:1. https://doi.org/10.1186/s41824-017-0019-6.
24. Papp L, Spielvogel CP, Rausch I, Hacker M, Beyer T. Personalización de la medicina a través de imágenes híbridas y análisis de Big Data médico. Front Phys 2018;6. https://doi.org/10.3389/fphy.2018.00051.
25. Milchenko M, Marcus D. Oscurecer la anatomía de la superficie en datos de imágenes volumétricas. Neuroinform 2013;11:65–75. https://doi.org/10.1007/s12021-012-9160-3.
228. Kesner A, Koo P. Una consideración para cambiar nuestras prácticas de ahorro de datos de PET: un análisis de costo/beneficio. J Nucl Med 2016; 57:1912-1912.
26. Allen B, Seltzer SE, Langlotz CP, Dreyer KP, Summers RM, Petrick N, et al. Una hoja de ruta para la investigación traslacional sobre inteligencia artificial en imágenes médicas: de los Institutos Nacionales de Salud/RSNA/ACR/The Academy Workshop 2018. Journal of the American College of Radiology 2019;16:1179–89. https://doi.org/10.1016/j.jacr.2019.04.014.
27. Avanzo M, Stancanello J, Naqa IE. Más allá de la imagen: la promesa de la radiomica. Physica Medica: European Journal of Medical Physics 2017;38:122–39. https://doi.org/10.1016/j.ejmp.2017.05.071.
28. Litjens G, Kooi T, Bejnordi BE, Setio AAA, Ciompi F, Ghafoorian M, et al. Una encuesta sobre el aprendizaje profundo en el análisis de imágenes médicas. Análisis de imágenes médicas 2017;42:60–88. https://doi.org/10.1016/j.media.2017.07.005.
29. Zhang C, Bengio S, Hardt M, Recht B, Vinyals O. La comprensión del aprendizaje profundo requiere repensar la generalización. ArXiv:161103530 [Cs] 2017.
30. Wolpert DH, Macready WG. No hay teoremas de almuerzo gratis para la optimización. IEEE Transactions on Evolutionary Computation 1997;1:67–82. https://doi.org/10.1109/4235.585893.
31. Yu-Chi Ho, Pepyne DL. Simple explicación del teorema de optimización sin almuerzo gratis. Actas de la 40a Conferencia IEEE sobre Decisión y Control (Cat. No.01CH37228), vol. 5, 2001, págs. 4409–14 vol.5. https://doi.org/10.1109/CDC.2001.980896.
32. Mohseni S, Zarei N, Ragan ED. Una encuesta y marco multidisciplinario para el diseño y la evaluación de sistemas de IA explicables. ArXiv:18111839 [Cs] 2020. 10.1145/3387166.
33. Li T, Tang W, Zhang L. El análisis de validación cruzada de Monte Carlo examina la vía de la diafonía asociada con la enfermedad de Parkinson. Neurol Sci 2016; 37:1327–33. https://doi.org/10.1007/s10072-016-2595-9.
34. Sollini M, Antunovic L, Chiti A, Kirienko M. Hacia la aplicación clínica de la minería de imágenes: una revisión sistemática de la inteligencia artificial y la radiomética. Eur J Nucl Med Mol Imaging 2019;46:2656–72. https://doi.org/10.1007/s00259-019-04372-x.
35. Hatt M, Lucia F, Schick U, Visvikis D. Validación multicéntrica de los hallazgos radiómicos: retos y oportunidades. EBioMedicine 2019;47:20–1. https://doi.org/10.1016/j.ebiom.2019.08054.
36. Park SH, Han K. Guía metodológica para la evaluación del rendimiento clínico y el efecto de la tecnología de inteligencia artificial para el diagnóstico y la predicción médica. Radiology 2018;286:800–9. https://doi.org/10.1148/radiol.2017171920.
37. Rudin C. Deje de explicar los modelos de aprendizaje automático de la caja negra para tomar decisiones de alto riesgo y utilice modelos interpretables en su lugar. Nature Machine Intelligence 2019;1:206–15. https://doi.org/10.1038/s42256-019-0048-x.
38. Nensa F, Demircioglu A, Rischpler C. Inteligencia Artificial en Medicina Nuclear. J Nucl Med 2019;60:29S-37S. https://doi.org/10.2967/jnumed.118.220590.
39. Zaharchuk G, Gong E, Wintermark M, Rubin D, Langlotz CP. El aprendizaje profundo en la neuroradiología. AJNR Am J Neuroradiol 2018;39:1776–84. https://doi.org/10.3174/ajnr.A5543.
40. Catana C. El amanecer de una nueva era en imágenes de PET de dosis baja. Radiology 2019;290:657–8. https://doi.org/10.1148/radiol.2018182573.
41. Guo J, Gong E, Fan AP, Goubran M, Khalighi MM, Zaharchuk G. Predecir mapas de flujo sanguíneo cerebral PET 15O-Agua a partir de resonancia magnética multicontraste utilizando una red neuronal convolucional profunda con evaluación del sesgo de cohorte de entrenamiento: Journal of Cerebral Blood Flow & Metabolism 2019. https://doi.org/10.1177/0271678X19888123.
42. Wei W, Poirion E, Bodini B, Durrleman S, Ayache N, Stankoff B, et al. Aprender contenido de mielina en la esclerosis múltiple de la resonancia magnética multimodal a través de la capacitación adversaria. ArXiv:180408039 [Cs] 2018; 11072:514–22. https://doi.org/10.1007/978-3-030-00931-1_59.
43. Hemmen HV, Massa H, Hurley S, Cho S, Bradshaw T, McMillan A. Un enfoque basado en el aprendizaje profundo para la corrección directa de la atenuación de PET de todo el cuerpo. J Nucl Med 2019; 60:569–569.
44. Hainc N, Federau C, Stieltjes B, Blatow M, Bink A, Stippich C. El brillante y artificial futuro de la lectura de neuroimagenes aumentada por la inteligencia artificial. Front Neurol 2017;8. https://doi.org/10.3389/fneur.2017.00489.
45. Menze BH, Jakab A, Bauer S, Kalpathy-Cramer J, Farahani K, Kirby J, et al. El Benchmark Multimodal De Segmentación De Imágenes Tumorales Del Tumor (BRATS). IEEE Transactions on Medical Imaging 2015;34:1993–2024. https://doi.org/10.1109/TMI.2014.2377694.
46. Armato SG, McLennan G, Bidaut L, McNitt-Gray MF, Meyer CR, Reeves AP, et al. El Consorcio de Bases de Datos de Imágenes Pulmonares (LIDC) y la Iniciativa de Recursos de Base de Datos de Imágenes (IDRI): una base de datos de referencia completa de nódulos pulmonares en tomografías computarizadas. Med Phys 2011;38:915–31. https://doi.org/10.1118/1.3528204.
47. Maier O, Menze BH, von der Galentz J, Ḧani L, Heinrich MP, Liebrand M, et al. ISLES 2015 – Un punto de referencia de evaluación pública para la segmentación de lesiones de accidente cerebrovascular isquémico de la resonancia magnética multiespectral. Med Image Anal 2017;35:250–69. https://doi.org/10.1016/j.media.2016.
48. Kistler M, Bonaretti S, Pfahrer M, Niklaus R, Büchler P. La base de datos de esqueletos virtuales: un repositorio de acceso abierto para la investigación y colaboración biomédica. J Med Internet Res 2013;15. https://doi.org/10.2196/jmir.2930.
49. Kim J, Lee B. Identificación de la enfermedad de Alzheimer y deterioro cognitivo leve utilizando una máquina de aprendizaje extremo jerárquica escasa multimodal. Human Brain Mapping 2018;39:3728–41. https://doi.org/10.1002/hbm.24207.
50. Katako A, Shelton P, Goertzen AL, Levin D, Bybel B, Aljuaid M, et al. El aprendizaje automático identificó un patrón de FDG-PET relacionado con la enfermedad de Alzheimer que también se expresa en la demencia con cuerpos de Lewy y la demencia de la enfermedad de Parkinson. Scientific Reports 2018;8:13236. https://doi.org/10.1038/s41598-018-31653-6.
51. Liu M, Cheng D, Yan W, Iniciativa de Neuroimagen de la Enfermedad de Alzheimer. Clasificación de la enfermedad de Alzheimer por combinación de redes neuronales convolucionales y recurrentes utilizando imágenes de FDG-PET. Front Neuroinform 2018;12:35. https://doi.org/10.3389/fninf.2018.00035.
52. Ding Y, Sohn JH, Kawczynski MG, Trivedi H, Harnish R, Jenkins NW, et al. Un modelo de aprendizaje profundo para predecir un diagnóstico de la enfermedad de Alzheimer mediante el uso de 18F-FDG PET del cerebro. Radiology 2019;290:456–64. https://doi.org/10.1148/radiol.2018180958.
53. Kim DH, Con Wit H, Thurston M. Inteligencia artificial en el diagnóstico de la enfermedad de Parkinson a partir de ioflupano-123 de emisión de un solo fotón de tomografía computarizada de exploración de transportador de dopamina utilizando el aprendizaje de transferencia. Nucl Med Commun 2018;39:887–93. https://doi.org/10.1097/MNM.0000000000000890.
54. Papp L, Pötsch N, Grahovac M, Schmidbauer V, Woehrer A, Preusser M, et al. Predicción de supervivencia de glioma con análisis combinado de características de PET in vivo 11C-MET, características ex vivo y características del paciente por aprendizaje automático supervisado. J Nucl Med 2018;59:892–9. https://doi.org/10.2967/jnumed.117.202267.
55. Xiong J, Yu W, Ma J, Ren Y, Fu X, Zhao J. El papel de las características radiómicas basadas en PET en la predicción del control local del cáncer de esófago tratado con quimiorradioterapia concurrente. Scientific Reports 2018;8:9902. https://doi.org/10.1038/s41598-018-28243-x.
56. Milgrom SA, Elhalawani H, Lee J, Wang Q, Mohamed ASR, Dabaja BS, et al. Un modelo de PET Radiomics para predecir el linfoma de Hodgkin mediastínico refractario. Sci Rep 2019;9:1322. https://doi.org/10.1038/s41598-018-37197-z.
57. Lucia F, Visvikis D, Vallières M, Desseroit M-C, Miranda O, Robin P, et al. Validación externa de un modelo combinado de PET y radiomics de resonancia magnética para la predicción de la recurrencia en pacientes con cáncer cervical tratados con quimiorradioterapia. Eur J Nucl Med Mol Imaging 2019;46:864–77. https://doi.org/10.1007/s00259-018-4231-9.
58. Abadi M, Barham P, Chen J, Chen Z, Davis A, Dean J, et al. TensorFlow: Un sistema para el aprendizaje automático a gran escala n.d.:21.https://doi.org/10.48550/arXiv.1605.08695
59. Te soy K. Documentación de Keras: Keras FAQ 2015. https://keras.io/getting_started/faq/#how-should-i-cite-keras (consultado el 10 de agosto de 2020).
60. Ketkar N. Deep Learning con Python: una introducción práctica. Apress; 2017. https://doi.org/10.1007/978-1-4842-2766-4.
61. Griethuysen JJM van, Fedorov A, Parmar C, Hosny A, Aucoin N, Narayan V, et al. Sistema de radiómica computacional para decodificar el fenotipo radiográfico. Cancer Res 2017;77:e104–7. https://doi.org/10.1158/0008-5472. CAN-17-0339.
62. Nioche C, Orlhac F, Boughdad S, Reuzé S, Goya-Outi J, Robert C, et al. LIFEx: Un cálculo de características radiomatrices para software gratuito en imágenes multimodales para acelerar los avances en la caracterización de la heterogeneidad tumoral. Cancer Res 2018;78:4786–9. https://doi.org/10.1158/0008-5472. CAN-18-0125.
63. Götz M, Nolden M, Maier-Hein K. Fenotipado MITK: Una cadena de herramientas de código abierto para la medicina personalizada basada en imágenes con radiomics. Radiother Oncol 2019; 131:108–11. https://doi.org/10.1016/j.radonc.2018.11.021.
64. Parekh VS, Jacobs MA. MPRAD: Un Marco De Radiómica Multiparamétrica. Breast Cancer Res Treat 2020; 180:407–21. https://doi.org/10.1007/s10549-020-05533-5.
65. Pedregosa F, Varoquaux G, Gramfort A, Michel V, Thirion B, Grisel O, et al. Scikit-learn: Aprendizaje automático en Python. Revista de Investigación de Aprendizaje Automático 2011; 12:2825–30.
66. Therneau T, Atkinson B, puerto BR (productor de la inicial R, mantenedor 1999-2017). rpart: Recursive Partitioning and Regresion Trees. 2019.
67. Kuhn M. Construir modelos predictivos en R Usando el paquete de cuidado. Journal of Statistical Software 2008;28:1–26. https://doi.org/10.18637/jss.v028.i05.
68. Papp L, Rausch I, Grahovac M, Hacker M, Beyer T. Extracción de características optimizada para el análisis radiómico de imágenes de PET 18F-FDG. J Nucl Med 2019;60:864–72. https://doi.org/10.2967/jnumed.118.217612.
69. Orlhac F, Boughdad S, Philippe C, Stalla-Bourdillon H, Nioche C, Champion L, et al. Un método de armonización posterior a la reconstrucción para estudios radiómicos multicéntricos en PET. J Nucl Med 2018;59:1321–8. https://doi.org/10.2967/jnumed.117.199935.
70. Zhu J-Y, Park T, Isola P, Efros AA. Traducción De Imagen A Imagen Sin Emparejar Utilizando Redes Adversarias De Ciclo Consistente. Conferencia Internacional IEEE 2017 sobre Visión por Computadora (ICCV), Venecia: IEEE; 2017, p. 2242–51. https://doi.org/10.1109/ICCV.2017.244.
71. Shin H-C, Tenenholtz NA, Rogers JK, Schwarz CG, Senjem ML, Gunter JL, et al. Síntesis de imágenes médicas para el aumento de datos y la anonimización mediante redes de adversarios generativos. ArXiv:180710225 [Cs, Stat] 2018.10.48550/arXiv.1807.10225
72. Pan SJ, Yang Q. Una encuesta sobre el aprendizaje de transferencia. IEEE Transactions on Knowledge and Data Engineering 2010;22:1345–59. https://doi.org/10.1109/TKDE.2009.191.
73. Shin H-C, Roth HR, Gao M, Lu L, Xu Z, Nogues I, et al. Redes neuronales convolucionales profundas para la detección asistida por computadora: arquitecturas de CNN, características de conjunto de datos y aprendizaje de transferencia. IEEE Trans Med Imaging 2016;35:1285–98. https://doi.org/10.1109/TMI.2016.2528162.
74. McCollough CH, Leng S, Yu L, Cody DD, Boone JM, McNitt-Gray MF. Índice de dosis de TC y dosis de paciente: no son lo mismo. Radiology 2011;259:311–6. https://doi.org/10.1148/radiol.11101800
75. Zhang Q, Zhu S. Interpretabilidad visual para el aprendizaje profundo: una encuesta. Frontiers Inf Technol Electronic Eng 2018;19:27–39. https://doi.org/10.1631/FITEE.1700808.
76. Gilpin LH, Bau D, Yuan BZ, Bajwa A, Specter M, Kagal L. Explicar explicaciones: una visión general de la interpretabilidad del aprendizaje automático. ArXiv:180600069 [Cs, Stat] 2019.: 10.1109/DSAA.2018.00018
77. Hustinx R. La interpretación de imágenes centradas en el médico está desapareciendo, ¿por qué debería ser un médico de medicina nuclear? Eur J Nucl Med Mol Imaging 2019;46:2708–14. https://doi.org/10.1007/s00259-019-04371-y.
78. Begoli E, Bhattacharya T, Kusnezov D. La necesidad de cuantificación de la incertidumbre en la toma de decisiones médicas asistida por máquina. Nature Machine Intelligence 2019;1:20–3. https://doi.org/10.1038/s42256-018-0004-1.
79. Liu X, Faes L, Kale AU, Wagner SK, Fu DJ, Bruynseels A, et al. Una comparación del rendimiento del aprendizaje profundo con los profesionales de la salud en la detección de enfermedades a partir de imágenes médicas: una revisión sistemática y un metaanálisis. The Lancet Digital Health 2019;1:e271–97. https://doi.org/10.1016/S2589-7500(19)30123-2.
80. Ribeiro MT, Singh S, Guestrin C. “¿Por qué debería confiar en ti?”: Explicando las predicciones de cualquier clasificador. ArXiv:160204938 [Cs, Stat] 2016. https://doi.org/10.48550/arXiv.1602.04938
81. Avati A, Jung K, Harman S, Downing L, Ng A, Shah NH. Mejorar los cuidados paliativos con el aprendizaje profundo. ArXiv:171106402 [Cs, Stat] 2017.10.1186/s12911-018-0677-8
Nuestros asesores
están para tu servicio
Privacidad
- CONTACTo
- Aviso de privacidad
- Aviso Legal
Mapa del sitio
- inicio
- Servicios
- Estudios
- Presentación
- BLOG
Contacto
- 01 (777) 314 3 54
- contact@gamagrafia.com.mx
- Paseo Cancún No 85 - 2 Col. Quintana Roo Cuernavaca, Morelos.
- © Todos los Derechos Reservados | Design by Business Club
- Aviso de Privacidad