Capítulo 15
Principios de las modalidades de radiología:
imágenes de resonancia magnética
Los átomos con un número impar de protones y/o un número impar de neutrones, poseen un momento angular de espín que simplemente se conoce como espín. Cualitativamente, estos giros se pueden visualizar como esferas cargadas giratorias que dan lugar a pequeños momentos magnéticos, una pila de agujas de brújula que apuntan aleatoriamente a lo largo de todas las direcciones espaciales. Cuando los espines están expuestos a un campo magnético estático, se orientan a lo largo de las líneas de campo magnético, similares a las agujas de la brújula, y crean un momento magnético neto. Tan pronto como el momento magnético neto se aleja de la dirección del campo magnético estático, que denotamos B0, el vector de magnetización efectivo precede en el plano transversal ortogonal a la dirección del campo magnético estático. Este es el fenómeno de resonancia magnética nuclear (RMN) descubierto por Felix Bloch y Edward Purcell en 1946.
La resonancia magnética (MRI) añade dimensiones espaciales a un experimento de 1D-RMN y permite señales de RMN resueltas espacialmente. Debido a su contraste de tejidos blandos y no invasividad, la resonancia magnética se ha convertido en un método estándar en el diagnóstico médico. El principio básico de la resonancia magnética es que la frecuencia de precesión de los espínes nucleares en un campo magnético estático, también denominado frecuencia Larmor, puede hacerse una función del espacio mediante la aplicación de gradientes de campo magnético lineal en tres direcciones ortogonales. Esta idea fue publicada por Sir Peter Mansfield y Paul C. Lauterbur en 1973, y recibieron el Premio Nobel de Fisiología o Medicina por este concepto en 2002 [1,2]. La relación entre la frecuencia Larmor de los espines y sus coordenadas espaciales en presencia de un gradiente magnético es la ecuación básica de la formación de imágenes:
ω(r)= γB 0 + γG·r (Eq. 1)
Vale la pena señalar que la frecuencia de Larmor, ω, solo se modifica efectivamente por componentes de campo de 0gradiente adicionales paralelos a B 0, ya que los campos de gradiente son varios órdenes de magnitud menores que B 0 (γG < < B 0). Los campos de gradiente horizontales inclinan ligeramente la dirección del campo neto, pero no influyen en la frecuencia de Larmor en aplicaciones estándar.
Considerando los espíns nucleares dentro de un campo de gradiente externo G en la posición espacial r con un volumen de muestra dV y la densidad de espín local ρ(r), la señal de MR dS de los espíns puede expresarse mediante:
d S(G,t) ~ ρ(r)d V exp(iω(r)t) (Eq. 2)
Esta aproximación descuida cualquier efecto de relajación. Se mantiene para gradientes fuertes asegurando que la dispersión de fase γ G · r sea mucho más rápida que la disminución de la relajación. Teniendo en cuenta la dependencia espacial de la frecuencia Larmor por gradientes de campo externos, la ecuación 2 puede escribirse como:
d S(G,t) ~ ρ(r)d V exp(i[γB 0 + γ G · r]tt) (Eq. 3)
En el caso de que la frecuencia de referencia del receptor se establezca en la frecuencia Larmor ω 00, la ecuación de señal de MRI integrada se convierte en:
S(t)= ρ(r)exp(iγ G · r t)d r (Eq. 4)
Esta ecuación de señal tiene la forma de una transformación de Fourier que se hace más clara cuando se introduce el concepto del vector espacial recíproco, indicado como k. k es la variable conjugada del vector espacial real rr:
k = γ G t (Eq. 5)
Por lo tanto, obtenemos una relación de Fourier entre la intensidad de la señal S(k) y la densidad de espín ρ(r):
S(k)=∫∫∫ ρ(r) exp(i2π kr)d r
ρ(r)=∫∫∫ (k) exp(-i2π kr)d k (Eq. 6)
El primer paso para obtener una imagen de densidad de espín en el espacio real es el mapeo del espacio inverso, también denotado como espacio k. El movimiento a través del espacio k puede ocurrir variando el tiempo t después de que se encendió un gradiente o cambiando la amplitud de gradiente G. La dirección de gradiente determina la dirección de la trayectoria a través del espacio k. Una vez completado el mapeo del espacio k, una transformación de Fourier revela la imagen en el espacio real. Este principio se muestra en la figura 1 para un gradiente lineal a lo largo de la dirección x, que codifica espacialmente la distribución de giro en la dirección x durante la adquisición de un FID. Debido a que la codificación espacial de los espíns se logra a través de modulaciones de la frecuencia de Larmor, este principio también se conoce como codificación de frecuencia.
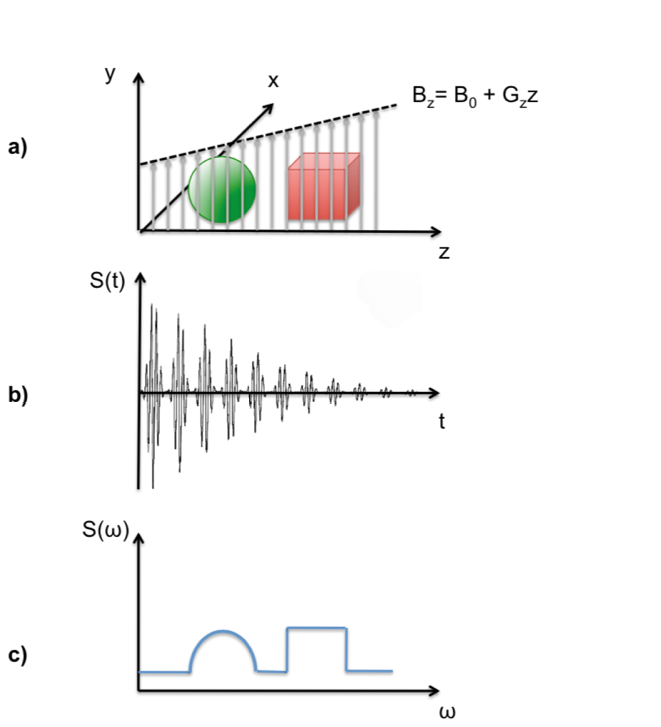
Un campo magnético externo B1 de una bobina de radiofrecuencia (RF) sintonizada a la frecuencia Larmor puede inclinar el vector de magnetización eficaz de los giros al plano transversal con su precesión siendo detectable como una señal en el intervalo de radiofrecuencia. Si se aplica un gradiente adicional perpendicular al gradiente de codificación de frecuencia, el pulso B1 es simplemente espínes excitantes que coinciden con su ancho de banda de frecuencia. Este procedimiento se llama excitación selectiva, en contraste con la excitación no selectiva sin un gradiente adicional. La selección de corte se utiliza principalmente para obtener imágenes de cortes individuales dentro del objeto bajo investigación. Para excitar selectivamente una porción de espesor ∆x, se requiere un ancho de banda de pulso de γG ∆x. El ancho de banda de frecuencia de pulso de RF es inversamente proporcional a la duración del pulso. Para lograr una selección de corte con un perfil de excitación de frecuencia casi rectangular, la forma de pulso B 1 de elección es una función sinc, ya que la transformación de Fourier de una función sinc está cerca de una función rectangular.
Después de una excitación selectiva de una losa de espines (por ejemplo, en la dirección z), la reconstrucción de una imagen en el espacio real se logra mediante una transformación bidimensional de Fourier. La codificación de frecuencia de la señal FID puede proporcionar una dimensión en el espacio k, que ahora denotaremos como la dirección x por conveniencia. El gradiente G x, que está presente durante un período de lectura t o durante el muestreo del FID, se denomina gradiente de lectura. La separación entre los puntos kx mapeados sucesivamente está determinada por una combinación del denominado tiempo de permanencia td, que es la diferencia de tiempo entre dos puntos de datos adquiridos del FID, y la intensidad del gradiente de lectura. La magnitud de kx para un punto específico en el espacio k está determinada por el número de índice n que varía de -N/2 a N/2 y N es el número máximo de puntos muestreados en una dirección en el espacio k:
(Eq.7)
Otras dimensiones en el espacio k se pueden mapear mediante codificación de fase. Aplicando otro gradiente G y en la dirección y durante un tiempo fijo antes de que comience el muestreo del FID, se impone una modulación de fase en los giros a lo largo del eje y. Por lo general, el gradiente se activa durante un tiempo fijo t ph de modo que el desplazamiento de fase debido al gradiente se convierte en:
∆Φ = γ t ph ∆G y (Eq.8)
El mapeo del espacio k en la dirección ky se lleva a cabo entonces variando la intensidad de gradiente G yy:
(Eq.9)
Con esta combinación de codificación de frecuencia y fase, cada FID durante una etapa de codificación de fase dada proporciona una línea en el espacio k. Al variar la fuerza de gradiente G y construimos una cuadrícula cartesiana 2D en el espacio k. Una vez que se mapea todo el espacio k, una transformada bidimensional de Fourier reconstruye la imagen espacial real ρ(r). La figura 2 ilustra una secuencia de formación de imágenes 2D estándar y el principio de muestreo de espacio k.
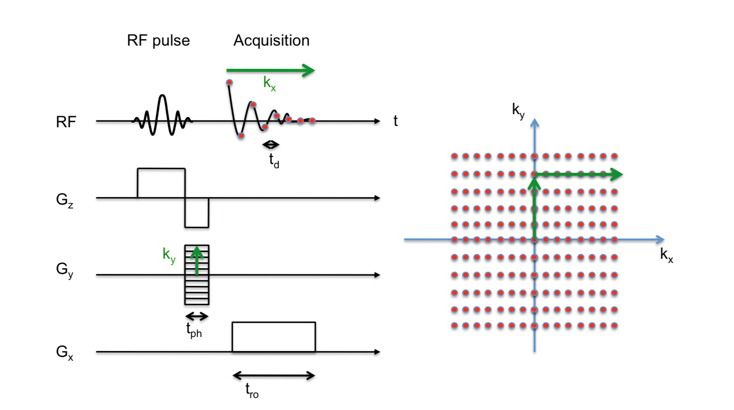
Se puede lograr un alto contraste de tejido blando en la MRI, debido a que la señal de MRI depende de la temporización y los ángulos de punta de la excitación utilizada para la generación de señal, así como de las propiedades de relajación de la magnetización longitudinal y transversal, con sus respectivas constantes de relajación T1 y T2.
Instrumentación
Un escáner de resonancia magnética consta de tres componentes principales: el imán, las bobinas de gradiente y las bobinas de RF para la transmisión y recepción de las señales de resonancia magnética. Actualmente se utilizan tres tipos de imanes: imanes permanentes, imanes resistivos e imanes superconductores. Los escáneres clínicos suelen utilizar un imán superconductor en el intervalo de 1,5-3 T y mantener una homogeneidad del campo B 0 por debajo de 4 ppm dentro de una región esférica de 50 cm de diámetro[3]. Los gradientes de campo magnético lineal a lo largo de la dirección x, y y z del imán se montan concéntricamente dentro del orificio del imán, permiten la codificación espacial de las señales de resonancia magnética y se utilizan para la cuña. Cada vez, la posición de la cama se mueve para un cuerpo completo MR, las corrientes de cuña se ajustan automáticamente para mejorar la homogeneidad de B 0. Típicamente, los espines nucleares se excitan usando una bobina de volumen de transmisión de cuerpo completo montada dentro del orificio del imán creando un campo magnético variable en el tiempo B1 (del orden de varios mT) en resonancia con la frecuencia Larmor. Típicamente, dicha bobina de volumen proporciona B1 uniforme a través de toda la región homogénea del imán. La sensibilidad de una adquisición de MRI depende de la distancia entre la bobina y la región que se está examinando y la geometría de la bobina. Cuanto más cerca se puede acercar la bobina al objeto medido y mejor coinciden las dimensiones de la bobina con la región de interés, mayor es la sensibilidad. Por lo tanto, se han desarrollado bobinas de radiofrecuencia dedicadas para una variedad de preguntas clínicas. Las bobinas diseñadas para PET/MR simultáneo difieren de las bobinas solo de MR en su diseño en dos elementos clave: en primer lugar, están diseñadas para minimizar las interferencias de radiofrecuencia con la electrónica de PET y, en segundo lugar, la cantidad de material se reduce tanto como sea posible, con el fin de minimizar la dispersión de γ-fotón y la atenuación para la cuantificación de la imagen de PET. Hay bobinas específicas para aplicaciones mamarias, de arteria carótida, pulmones, columna vertebral, próstata, rodilla, neonatales y multinucleares, entre otras. Las bobinas receptoras también se pueden usar como matrices en fase que permiten la aceleración de adquisiciones de imágenes de gran volumen.
Enfoques complementarios de resonancia magnética y PET para aplicaciones médicas
Hay un número importante de aplicaciones en oncología, neurología, cardiología y especialmente imágenes pediátricas donde la resonancia magnética en combinación con PET simultánea o posterior podría proporcionar beneficios significativos sobre PET/TC y exploraciones individuales de PET y MRI. En comparación con PET/CT, PET/MR expone al paciente a menos radiación, permite un alto contraste de tejidos blandos e información multiparamétrica que se puede explotar de diferentes maneras. En comparación con las resonancias magnéticas individuales y las exploraciones PET, es posible realizar MR-PET simultánea en una sola sesión, mientras que, utilizando escáneres individuales, generalmente se deben coordinar dos exámenes, lo que tiene un impacto adicional en la logística general y también en la comodidad del paciente. El co-registro cuasi-perfecto entre la información anatómica y funcional es siempre un beneficio de PET/MR simultáneo en comparación con el PET/MR secuencial, para el que el remuestreo o registro entre las imágenes de PET y MRI puede introducir potencialmente errores. En el caso de pacientes sensibles, como en imágenes pediátricas o para pacientes con potencial reproductivo, la evitación de la exposición a la radiación TC es un beneficio importante de la PET/RM.
Enfoques de IA para acortar los tiempos de adquisición de la resonancia magnética
También en la IRM, los enfoques de IA se utilizan cada vez más para acortar los tiempos de adquisición de MRI sin comprometer la calidad de la imagen. Uno de los enfoques más impactantes es la reconstrucción de imágenes basada en el aprendizaje profundo, donde las redes neuronales generan imágenes de alta calidad a partir de datos en bruto submuestreados (k-space). Esto permite un escaneo significativamente más rápido. Soluciones comerciales como “AIR Recon DL” de GE, “Deep Resolve” de Siemens y “AiCE” de Canon ya están en uso clínico.
La superresolución también está ganando terreno: las imágenes de baja resolución adquiridas rápidamente son ampliadas por la IA a una calidad de alta resolución cercana, que es especialmente útil en imágenes cerebrales o musculoesqueléticas. Los algoritmos de corrección de movimiento basados en IA reducen aún más el tiempo de escaneo efectivo al corregir los artefactos de movimiento, minimizando así la necesidad de repetir escaneos, un beneficio importante en pacientes pediátricos o ancianos.
Una aplicación adicional de IA es la optimización automatizada del protocolo, donde la IA selecciona los parámetros óptimos de escaneo antes de la adquisición, lo que simplifica los protocolos para obtener imágenes más rápidas y eficientes.
En conjunto, estos métodos contribuyen a exámenes más cortos, mayor comodidad del paciente y una utilización más eficiente de los escáneres [5, 6] Mientras que los desafíos persisten, como la aprobación regulatoria (regulación de dispositivos médicos, aprobación CE y FDA), los requisitos del conjunto de datos y la integración clínica, la IA tiene un gran potencial para mejorar fundamentalmente los flujos de trabajo y la accesibilidad de la resonancia magnética.
2. PC Lauterbur. Formación de imágenes por interacciones locales inducidas: ejemplos que emplean resonancia magnética nuclear. Nature 1973;242:190–1. https://doi.org/10.1038/242190a0.
3. Vandenberghe S, Marsden PK. PET-MRI: una revisión de los desafíos y soluciones en el desarrollo de imágenes multimodales integradas. Phys Med Biol 2015;60:R115-154. https://doi.org/10.1088/0031-9155/60/4/R115
4. Akçakaya M, Moeller S, Weingärtner S, Uğurbil K. Redes artificiales-neurales robustas específicas para la reconstrucción de la interpolación del espacio k (RAKI): aprendizaje profundo sin base de datos para imágenes rápidas. Resonancia magnética en Med [Internet]. 2019 Ene [citado el 20 de octubre de 2025];81(1):439–53. Disponible en: https://onlinelibrary.wiley.com/doi/10.1002/mrm.27420
5. Heckel R, Jacob M, Chaudhari A, Perlman O, Shimron E. Aprendizaje profundo para la reconstrucción acelerada y robusta de la resonancia magnética. Magn Reson Mater Phy [Internet]. 2024 23 de julio [citado en 2025 Oct 20]; 37(3):335–68. Disponible en: https://link.springer.com/10.1007/s10334-024-01173-8
6. Chen Y, Schönlieb CB, Liò P, Leiner T, Dragotti PL, Wang G, et al. Reconstrucción basada en IA para resonancia magnética rápida — Una revisión sistemática y meta-análisis [Internet]. arXiv; 2021 [citado en 2025 Oct 20]. Disponible en: https://arxiv.org/abs/2112.12744
Nuestros asesores
están para tu servicio
Privacidad
- CONTACTo
- Aviso de privacidad
- Aviso Legal
Mapa del sitio
- inicio
- Servicios
- Estudios
- Presentación
- BLOG
Contacto
- 01 (777) 314 3 54
- contact@gamagrafia.com.mx
- Paseo Cancún No 85 - 2 Col. Quintana Roo Cuernavaca, Morelos.
- © Todos los Derechos Reservados | Design by Business Club
- Aviso de Privacidad